Qué es Célula electroquímica ?
Una célula electroquímica es un dispositivo que transforma la energía química en energía eléctrica o viceversa, mediante reacciones redox. Estas celdas son fundamentales en aplicaciones como baterías, pilas de combustible y procesos de electroplating, donde se aprovechan los electrones liberados o consumidos para generar corriente eléctrica.
¿Qué significa celda electroquímica?
Una celda electroquímica es un dispositivo o mecanismo que puede generar energía eléctrica a partir de una reacción química o utilizar energía eléctrica para producir una reacción química.
Este es un concepto crucial en el estudio de la corrosión, porque la corrosión es un proceso electroquímico e involucra la formación de celdas electroquímicas.
El estudio de la formación de celdas electroquímicas puede ayudar a:
- Determinar la naturaleza de la degradación del material.
- Supervise y minimice las fallas debido a la corrosión
- Reducir el costo de reparaciones y reemplazos de componentes y piezas críticas
industriapedia explica la celda electroquímica
La corriente eléctrica puede ocurrir debido a ciertas reacciones químicas. Como sistema electroquímico se le conoce como celda galvánica o voltaica. Una batería de plomo-ácido es un ejemplo de tal sistema.
Cuando se suministra energía eléctrica a una celda electroquímica, por otro lado, el cambio químico que ocurre se conoce como electrólisis. Muchos metales como el aluminio se producen por electrólisis.
La corrosión, en muchos casos, ocurre debido a las celdas electroquímicas. La corrosión, como reacción electroquímica, se produce a través de una serie de reacciones redox, que también se observan en las baterías. Por lo general, el metal (como el acero) bajo ataque funciona como ánodo, se oxida y forma iones metálicos y electrones libres. Los electrones libres así formados reducen el oxígeno para formar hidróxido, produciendo una reacción catódica para asegurar la electro neutralidad.
La disolución del metal en el ánodo puede hacer que los iones metálicos entren en una solución o que los iones metálicos se acumulen en la superficie del material. En el primer caso, los iones metálicos pueden oxidarse aún más y se puede formar un hoyo. En el segundo caso, se puede formar un revestimiento de barrera y este delgado revestimiento de iones sólidos evita una mayor corrosión. La corrosión del aluminio suele seguir el segundo caso, ya que el revestimiento inicial de óxido de aluminio detiene o retarda la corrosión.
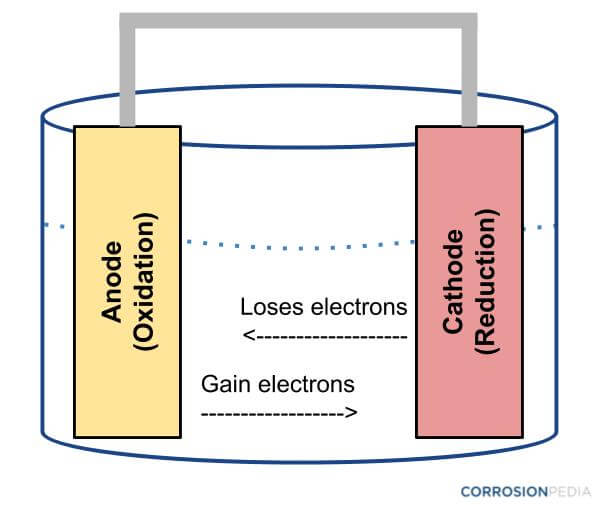
Figura 1. Diagrama de una celda electroquímica.
Una característica particular de la mayoría de los procesos de corrosión es que las etapas de reducción y oxidación ocurren en diferentes lugares del metal. Esto es posible gracias a la conductividad de los metales, que permite el flujo de electrones del ánodo al cátodo. Una capa de humedad es esencial para esta reacción electroquímica, a fin de transmitir iones hacia y desde el metal, ya que solo una capa muy delgada de vapor de agua adsorbido será adecuada. Así, el proceso de corrosión puede ser considerado y estudiado como el caso de una celda electroquímica en cortocircuito.
Por lo tanto, la generación de celdas electroquímicas precede a la mayoría de los tipos de deterioro corrosivo.
Las partes de las superficies que sirven como ánodos pueden depender de las tensiones residuales. Las moléculas en regiones que han tenido estrés residual durante la producción, a menudo tienen energías libres y, por lo tanto, pueden volverse anódicas de forma natural y atraer un ataque de corrosión temprano.

Novedades